Différence clé: L' émission est la capacité d'une substance à émettre de la lumière lorsqu'elle interagit avec la chaleur. L'absorption est l'opposé de l'émission, où l'énergie, la lumière ou le rayonnement sont absorbés par les électrons d'une matière particulière.
Les spectres d'émission et d'absorption sont des techniques utilisées en chimie et en physique. La spectroscopie est l'interaction du rayonnement et de la matière. En utilisant la spectroscopie, un scientifique peut déterminer la composition d’une matière donnée. C'est vraiment bénéfique de traiter des substances inconnues. Les spectres d'émission et d'absorption sont différents mais restent liés.

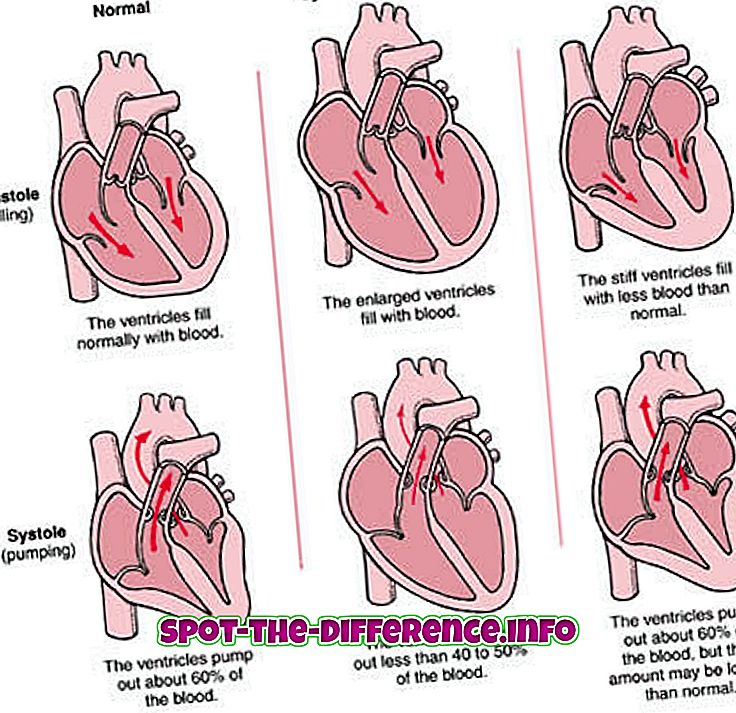
Chaque élément ou substance a un niveau d'émission unique ou la quantité d'énergie qu'il émet; Cela aide les scientifiques à identifier des éléments dans des substances inconnues. L'émission d'un élément est enregistrée sur un spectre d'émission ou un spectre atomique. L'émittance d'un objet mesure la quantité de lumière émise par celui-ci. La quantité d'émission d'un objet varie en fonction de la composition spectroscopique de l'objet et de la température. Les fréquences d'un spectre d'émission sont enregistrées en fréquences lumineuses, la couleur de la lumière déterminant la fréquence. Les fréquences peuvent être déterminées en utilisant la formule Ephoton = hv, où 'Ephoton' est l'énergie du photon, 'v' sa fréquence et 'h' la constante de Planck. L'émission peut se produire sous forme de lumière et de rayons, tels que gamma et radio. Le spectre est une longueur d’onde sombre avec des bandes de couleur, qui sert à déterminer l’émission de l’objet.
L’absorption est le contraire de l’émission, où l’énergie, la lumière ou le rayonnement est absorbé par le

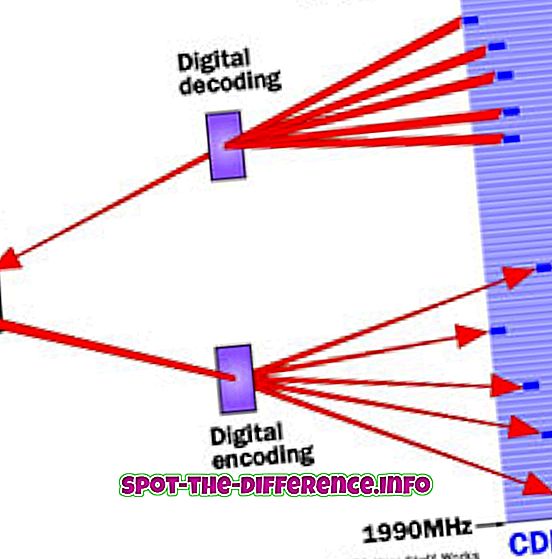
L'absorption est utilisée pour déterminer la présence d'une substance particulière dans un échantillon ou la quantité de la substance présente dans l'échantillon. Ils sont également utilisés en physique moléculaire et atomique, en spectroscopie astronomique et en télédétection. L'absorption est principalement déterminée par la composition atomique et moléculaire du matériau. Ils peuvent également dépendre de la température, du champ électromagnétique, de l'interaction entre les molécules de l'échantillon, de la structure cristalline dans les solides et de la température. Afin de déterminer le niveau d'absorption d'une substance, un faisceau de rayonnement est dirigé sur l'échantillon et l'absence de lumière réfléchie par l'objet peut être utilisée pour calculer l'absorption. Le spectre d'absorption est généralement de couleur claire, avec des bandes sombres qui le traversent. Ces bandes sombres sont utilisées pour déterminer l'absorption de l'objet.
Émission | Spectres d'absorption | |
La description | L'émission est la capacité d'une substance à émettre de la lumière lorsqu'elle interagit avec la chaleur. | L'absorption est l'opposé de l'émission, où l'énergie, la lumière ou le rayonnement sont absorbés par les électrons d'une matière particulière. |
Sujets | Chimie et Physique | |
Objectif | Peut être utilisé dans le cadre de la spectroscopie pour déterminer la composition d’une matière donnée. | Peut être utilisé dans le cadre de la spectroscopie pour déterminer le niveau d'absorption de certains objets et leur capacité à retenir la chaleur. Peut aussi être utilisé en physique moléculaire et atomique, en spectroscopie astronomique et en télédétection. |
Les types | - | Spectres d'absorption atomique et spectres d'absorption moléculaire. |
Effet sur les molécules | Lorsqu'une substance interagit avec la lumière, certaines de ses molécules absorbent la chaleur de la lumière et sont excitées. Cela les rend instables et ils essaient d'émettre l'excès d'énergie pour revenir à la normale. Les molécules excitées libèrent l'excès d'énergie sous forme de photons, également connus à particules légères. | Lorsqu'une substance interagit avec la lumière, certaines de ses molécules absorbent la lumière ou le rayonnement. Les types de longueur d'onde de la lumière absorbée peuvent être cartographiés. |
Résultat | Le type de photons émis permet de déterminer le type d’éléments constitutifs de la substance, chaque élément ou substance ayant un niveau d’émission unique ou la quantité d’énergie qu’il dégage. | Le type de longueur d'onde absorbée permet de déterminer la quantité de substance présente dans l'échantillon. |
En termes simples | Le spectre d'émission enregistre les longueurs d'onde émises par les matériaux, qui avaient été stimulés par l'énergie auparavant. | Les spectres d'absorption enregistrent les longueurs d'onde absorbées par le matériau |
Ressemble à | De couleur sombre, avec des bandes claires qui la traversent. Ces bandes de lumière permettent de déterminer les types de photons émis par l'objet. | De couleur claire, avec des bandes sombres qui la traversent. Ces bandes sombres sont utilisées pour déterminer l'absorption de l'objet. |
Unités | Les fréquences d'émission peuvent être déterminées en utilisant la formule Ephoton = hv, où 'Ephoton' est l'énergie du photon, 'v' sa fréquence et 'h' la constante de Planck. | Peut être tracé dans une longueur d'onde, une fréquence ou un nombre d'onde. |