Différence clé: La diffusion est le processus par lequel les molécules se déplacent et se déplacent d'un endroit à un autre sans nécessiter de mouvement important. L'effusion est le processus par lequel les molécules se déplacent dans un trou d'épingle d'un lieu de concentration élevée à une concentration faible.
Les termes diffusion et épanchement sont couramment utilisés dans de nombreuses sciences telles que la chimie, la physique et la biologie. En chimie, ces deux termes sont deux propriétés des gaz. Ces deux sont déroutants pour beaucoup de gens qui viennent d’apprendre les bases des gaz et de leurs propriétés. Diffusion et Effusion sont deux termes différents qui signifient deux choses différentes et ne doivent pas être utilisés de manière interchangeable. La diffusion fait référence à la capacité des gaz à se mélanger les uns aux autres, tandis que l'épanchement fait référence à la capacité des gaz à traverser un petit trou d'épingle. La diffusion est également utilisée en sociologie, économie et finance pour désigner la diffusion des personnes, des idées et des valeurs.
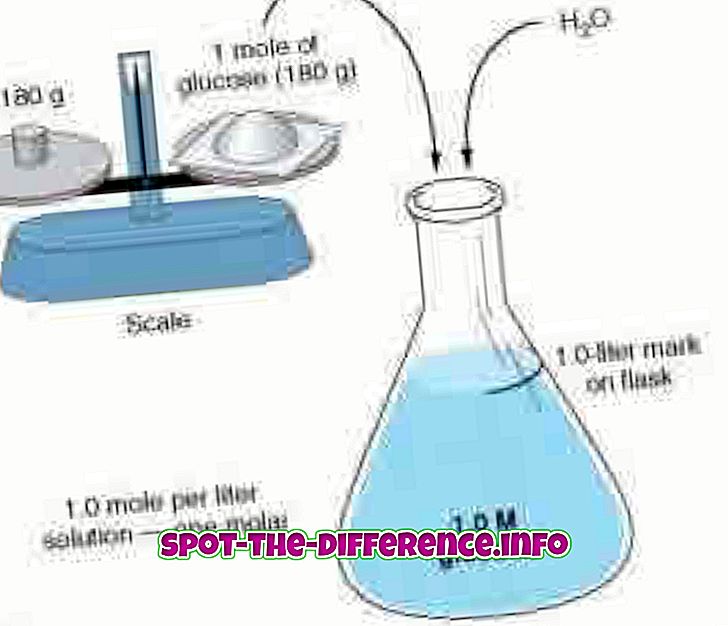
La diffusion est le processus par lequel les molécules se déplacent et se déplacent d'un endroit à un autre sans nécessiter de mouvement important. La diffusion entraîne le déplacement ou le mélange de molécules en utilisant uniquement l'énergie cinétique. Le mot "diffusion" est dérivé du mot latin "diffundere" qui signifie "étaler". En diffusion, les molécules sont dans un état de mouvement constant et lorsqu'elles sont propulsées par une énergie cinétique ou thermique, elles ont tendance à se mélanger à d'autres molécules, ce qui crée un mélange inséparable. Prenons une approche pratique: un conteneur est divisé en sections A & B à l’aide d’une partition solide; la première section est remplie d'eau, tandis que la deuxième section est remplie de colorant rouge. Maintenant, lorsque la cloison est soulevée, le colorant et l’eau tentent de remplir l’ensemble du récipient. Ensuite, le colorant souille lentement l'eau rouge, ce qui est diffusion.
La diffusion provoque le passage de molécules d'une zone de concentration supérieure à une zone de concentration inférieure, ce qui entraîne le mélange de toutes les molécules. La diffusion s'arrête lorsque toutes les molécules sont bien réparties. La diffusion ne se limite pas à l'eau et fonctionne mieux dans les états gazeux, où les molécules ont plus d'énergie et ont la capacité de se mélanger à d'autres molécules. Il existe deux approches de la diffusion: phénoménologique et atomistique. Selon l'approche phénoménologique, les molécules se déplacent des régions de concentration supérieure aux régions de concentration inférieure. Dans l’approche atomistique, la diffusion est considérée comme due à la marche aléatoire des particules diffusantes, dans laquelle la diffusion est propulsée par l’énergie thermique, ce qui entraîne leur mélange. La diffusion joue un rôle important dans la création des minéraux, des nutriments et de l'énergie nécessaires à l'organisme.

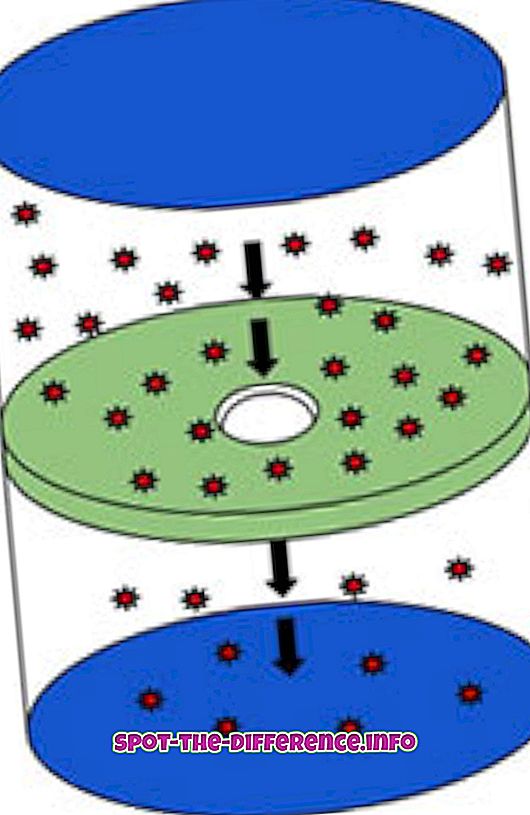
L'effusion est le processus par lequel les molécules se déplacent dans un trou d'épingle d'un lieu de concentration élevée à une concentration faible. Le processus décrit la capacité du gaz à traverser un petit trou sans collision entre les molécules. Cela se produit lorsque le diamètre du trou est considérablement plus petit que le libre parcours moyen des molécules. Le libre parcours moyen est la distance moyenne parcourue par une particule en mouvement entre des collisions successives. Un exemple pratique consiste à remplir un récipient avec une bouteille de fumée et à percer un petit trou dans la bouteille. La fumée qui sort du trou est considérée comme un épanchement.
Selon le chimiste écossais Thomas Graham, l'auteur de la formule de mesure de l'épanchement a créé une loi de Graham qui détermine la vitesse à laquelle le gaz circule et comment il peut être mesuré. Selon la loi de Graham, la vitesse à laquelle les gaz dégagés dépendent de leur poids moléculaire. Le gaz dont le poids moléculaire est inférieur dégagera plus rapidement qu'un gaz ayant un poids moléculaire supérieur. L'effusion est calculée en mesurant le nombre de molécules traversant le trou en une seconde. De même, en thermodynamique, la vitesse d'effusion d'un gaz est inversement proportionnelle à la racine carrée de la masse de ses particules.