Principale différence: les atomes sont les unités de base qui composent tout. Les atomes sont minuscules, allant de 0, 1 à 0, 5 nanomètres de large. Chaque atome d'un élément est composé de protons, neutrons et électrons. Les atomes de différents éléments se rassemblent pour former des molécules. Cela se produit via une réaction chimique. Une molécule est la plus petite quantité d'une substance chimique pouvant exister.
Un élément est une substance chimique pure possédant un ou plusieurs types d'atomes, qui se distingue par son numéro atomique. Le numéro atomique est dérivé du nombre de protons présents dans le noyau de l'élément. Au total, 118 éléments ont été identifiés, répartis entre le métal, les métalloïdes et les non-métaux. Chaque élément a son propre ensemble de propriétés. La plupart des éléments sont disponibles sur la Terre, tandis que quelques-uns ont été développés artificiellement par le biais de réactions nucléaires. Un élément est déjà dans sa forme la plus brute et ne peut plus être décomposé. Tous les éléments peuvent être trouvés dans le tableau périodique, classés par numéro atomique.
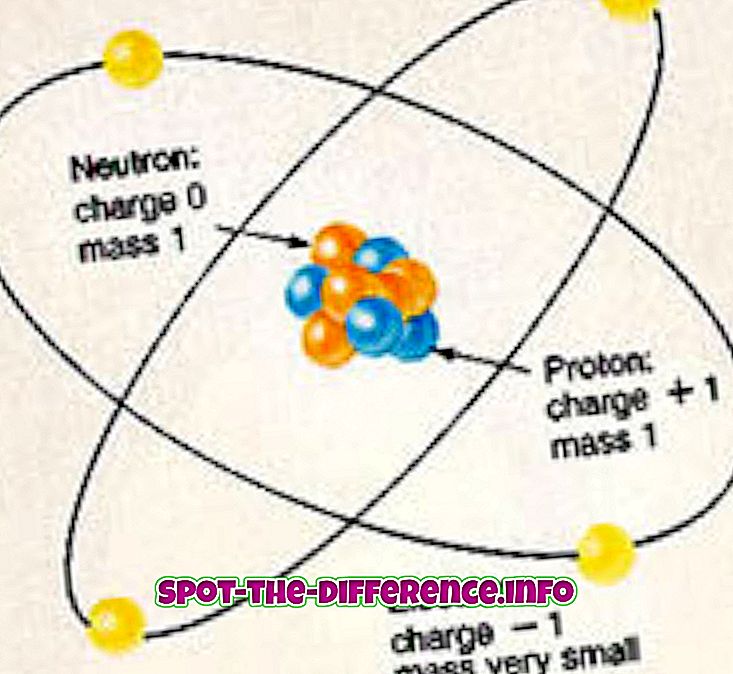
Chaque atome d'un élément est composé de protons, neutrons et électrons. Les protons et les neutrons constituent le noyau de l'atome et se situent au centre de l'atome. Le noyau est entouré d'un nuage d'électrons qui lui sont liés par une force électromagnétique. Les électrons ont une charge négative qui les attire vers le noyau, car les protons du noyau ont une charge positive. Les neutrons, par contre, n'ont pas de charge.
Le nombre de protons, de neutrons et d'électrons dans un atome détermine de quel élément il s'agit. Par exemple: Un atome de fer a 26 protons, 30 neutrons et 26 électrons. Chaque atome de fer aura cette configuration.
Les atomes de différents éléments se rassemblent pour former des molécules. Cela se produit via une réaction chimique. Par exemple, deux atomes d'hydrogène et un atome d'oxygène se combinent pour former une molécule d'eau.

Une molécule peut avoir des propriétés très différentes des éléments qui la composent. Par exemple: l'eau se comporte très différemment de l'oxygène ou de l'hydrogène, même si elle est composée de deux atomes d'hydrogène et d'un atome d'oxygène.
De plus, un atome ne peut exister indépendamment dans la nature sans se lier à quelque chose. Nous ne trouverons jamais qu'un seul atome d'oxygène ou un seul atome de carbone. Il est toujours lié à quelque chose, tel que O2 (oxygène) ou CO2 (dioxyde de carbone). Lorsqu'elle est liée à une molécule, la molécule peut exister de manière indépendante dans la nature. C'est pourquoi on peut toujours trouver une molécule d'oxygène, une molécule de dioxyde de carbone, une molécule d'eau (H2O), etc.
Dans une molécule, les atomes sont collés ensemble sous une forme ou une forme particulière. Cela dépend principalement du nombre de liaisons que l'atome peut créer. Les atomes forment des molécules en formant des liaisons chimiques les uns avec les autres. Les atomes d'oxygène ont toujours deux liaisons avec d'autres atomes, les atomes de carbone ont toujours quatre liaisons avec d'autres atomes et les atomes d'azote ont toujours trois liaisons avec d'autres atomes. De ce fait, un type de molécule particulier a toujours une forme particulière, telle que pentagonale, hexagonale, latérale, bilatérale, etc.
Les molécules ont toujours tendance à se regrouper, leur formation dépendant de leur état. Comme dans un état gazeux, les molécules ont tendance à voler. Dans un état liquide, les molécules ont tendance à être regroupées de manière lâche afin de pouvoir encore se déplacer. Alors que dans un état solide, les molécules sont étroitement emballées et ne peuvent que vibrer.
Les molécules sont généralement représentées dans une formule moléculaire. Par exemple: O2, H2O, CO2, C6H12O6 (sucre). La formule moléculaire est le nom de l'élément suivi du nombre d'atomes de cet élément dans la molécule.