Différence clé: l’ absorption est un phénomène général dans lequel un absorbant pénètre complètement dans le corps d’un solide ou d’un liquide pour former un composé ou une solution. Par ailleurs, l’adsorption est un phénomène de surface dans lequel les molécules d’un adsorbat ne se concentrent qu’à la surface d’un adsorbant.
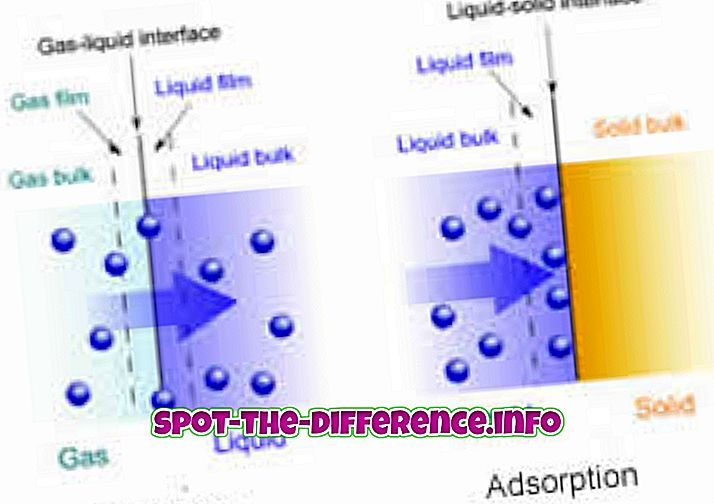
Réaction chimique - dioxyde de carbone absorbé par une solution de carbone potassique
Processus physique - Air absorbé dans l'eau en se dissolvant

Il existe deux types de modes d'adsorption: chimique et physique. En adsorption chimique, les molécules et la surface sont liées par de faibles forces de Vander Walls. D'autre part, dans l'adsorption chimique, une liaison chimique est formée entre les molécules et la surface.
Par conséquent, la principale différence entre l’absorption et l’absorption réside dans le fait que l’absorption est un phénomène général, c’est-à-dire qu’elle se produit dans l’ensemble du corps du matériau, alors que l’absorption reste un phénomène de surface. L'adsorption est toujours exothermique, tandis que l'absorption est endothermique. La sorption comprend à la fois les processus d'absorption et d'adsorption.
Comparaison entre l'adsorption et l'absorption:
Adsorption | Absorption | |
Définition | Accumulation d'un gaz ou d'un soluté liquide à la surface d'un solide ou d'un liquide | Diffusion d'une substance dans un liquide ou un solide pour former une solution ou un composé |
Exemple | Les gaz inertes sont adsorbés sur le charbon de bois. | Une éponge sèche absorbe l'eau |
Échange de chaleur | Exothermique à l'exception de l'adsorption de H2 sur le verre | Endothermique |
Atteindre l'équilibre | Comparativement plus rapide | Relativement lentement |
Concentration | La concentration à la surface de l'adsorbant est différente de celle de la masse | La concentration reste la même dans tout le matériau |
Taux d'occurrence | C'est rapide au début mais plus tard, son taux commence à baisser | Il se déroule à un taux uniforme |